Con el ensayo de la vacuna de AstraZeneca aún en pausa en EE. UU., Abundan las preguntas sobre las misteriosas enfermedades de los participantes del estudio
Mientras las autoridades de salud de EE. UU. Consideran si permitir que AstraZeneca reanude el ensayo clínico de su vacuna contra el coronavirus, quedan preguntas cruciales sobre las enfermedades neurológicas que sufren los participantes del estudio que recibieron inyecciones de la vacuna experimental.El ensayo ha estado en suspenso en los Estados Unidos durante más de dos semanas, y los reguladores enfrentan la tarea de intentar averiguar si estas enfermedades fueron aleatorias y desconectadas de la vacuna, o si están relacionadas con la vacuna.AstraZeneca y su socio, la Universidad de Oxford, han dado varios relatos de los voluntarios enfermos.AstraZeneca dijo a los medios de comunicación que el primer voluntario que se enfermó tenía “un caso no diagnosticado de esclerosis múltiple”, pero la información en el sitio web de Oxford describe voluntarios que desarrollaron “síntomas neurológicos inexplicables”. La empresa ha declarado que la segunda voluntaria tenía “una enfermedad inexplicable”, pero un documento interno de la empresa , que estaba etiquetado como “inicial”, afirma que al menos en un momento, tenía una rara enfermedad neurológica llamada mielitis transversa.”Esas son declaraciones muy diferentes”, dijo el Dr. Harlan Krumholz, profesor de la Facultad de Medicina de Yale, después de leer informes de AstraZeneca y Oxford sobre la condición del primer participante. “Su información debe ser coherente y, cuando no es coherente, surgen preguntas”.
Krumholz y otros científicos dijeron que la naturaleza de las enfermedades neurológicas de los participantes es importante. Si los dos sujetos del estudio tuvieran condiciones similares, eso generaría más preguntas sobre si la vacuna es la culpable. Si sus condiciones son diferentes, eso podría sugerir que fueron al azar y no el resultado de la vacuna.Mark Slifka, un inmunólogo, dijo que es particularmente preocupante porque la información publicada en el sitio web de Oxford dice que ambos participantes sufren enfermedades neurológicas.”Es por eso que esto es tan impactante para mí: ambas son enfermedades neurológicas, y eso en sí mismo es una señal de alerta”, dijo Slifka, profesor de la Universidad de Salud y Ciencias de Oregón.En su sitio web, Oxford escribió que las enfermedades de los voluntarios “se consideraba poco probable que estuvieran asociadas con la vacuna o no había pruebas suficientes para decir con certeza que las enfermedades estaban o no relacionadas con la vacuna”.El director ejecutivo de AstraZeneca, Pascal Soriot, dijo en un evento el jueves que “debemos colocar la seguridad en el centro de todo lo que haces”.
¿Enfermedad de los participantes relacionada o aleatoria?
El ensayo clínico de la vacuna contra el coronavirus de AstraZeneca ya se reanudó en otros países, incluido el Reino Unido. Un portavoz de la empresa dijo que están trabajando con los reguladores estadounidenses para reanudar los juicios en ese país también.”Seguimos trabajando con la FDA para facilitar la revisión de la información y la agencia decidirá cuándo se puede reanudar el ensayo en Estados Unidos”, escribió el portavoz en un correo electrónico.Un portavoz de la FDA se negó a comentar y refirió a CNN a AstraZeneca.El principal médico de enfermedades infecciosas del país le dijo a CNN el lunes que AstraZeneca y Oxford tendrán que estar atentos a cualquier otro voluntario que desarrolle síntomas similares.
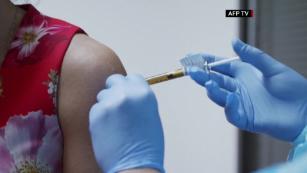
“Lo que esto desencadena es un estado de alerta adicional a medida que avanza el ensayo, si avanza, por parte de los sitios de ensayos clínicos para buscar algo incluso remotamente similar, para ver si hay casos adicionales”, dijo el Dr. Anthony. Fauci, director del Instituto Nacional de Alergias y Enfermedades Infecciosas. Slifka y otros científicos dijeron que están complacidos de que la FDA se esté tomando el tiempo para considerar si se debe permitir que el ensayo se reanude en Estados Unidos.”Tiene sentido que la FDA quiera seguir investigando”, dijo Slifka.Los portavoces de la Universidad de Oxford y los portavoces de AstraZeneca se negaron a responder preguntas específicas sobre los diferentes relatos de las enfermedades de los participantes.En su sitio web, Oxford señala que, al 12 de septiembre, “a nivel mundial, unas 18.000 personas han recibido las vacunas del estudio como parte del ensayo. En ensayos grandes como este, se espera que algunos participantes se sientan mal y todos los casos deben ser evaluados cuidadosamente. para garantizar una evaluación cuidadosa de la seguridad “.Un portavoz de Oxford también envió declaraciones a CNN.”Todos los investigadores y participantes del ensayo continuarán siendo actualizados con la información relevante, y esta solo se divulgará de acuerdo con los estándares regulatorios y del ensayo clínico. Estamos comprometidos con la seguridad de nuestros participantes y con los más altos estándares de conducta en nuestros estudios y seguirá vigilando de cerca la seguridad “, según otro comunicado de la universidad.En un comunicado, un portavoz de la universidad dijo que Oxford “no ofrece acceso a datos de pacientes individuales según las pautas de los ensayos clínicos”.AstraZeneca dijo a CNN que “para mantener la integridad del ensayo y proteger el derecho de privacidad de los pacientes inscritos en los ensayos, los eventos adversos graves se comunican a los investigadores del ensayo, a los comités independientes de monitoreo de seguridad de los datos y a las autoridades sanitarias durante el estudio. Es importante tener en cuenta que los eventos son evaluados y evaluados a lo largo del tiempo por estas partes a medida que se disponga de información adicional. Estos eventos deben informarse a las autoridades sanitarias y a los investigadores y pueden requerir actualizaciones de seguridad en el formulario de consentimiento y notificación a los pacientes en un protocolo continuo. Tales eventos pueden tener un impacto en el realización del estudio “.
El primer participante enfermo
AstraZeneca y la Universidad de Oxford anunciaron las dos enfermedades neurológicas a principios de este mes.En una hoja de información entregada a los participantes del estudio, la Universidad de Oxford menciona “voluntarios” que desarrollaron síntomas neurológicos, pero no especifica cuántos.Cuando CNN preguntó cuántos participantes del estudio habían desarrollado problemas neurológicos, AstraZeneca y la Universidad de Oxford se negaron a responder.De los dos participantes del estudio que se sabe que se enfermaron, la primera enfermedad ocurrió en julio.La condición de ese voluntario no se anunció hasta el 9 de septiembre, cuando AstraZeneca escribió en un correo electrónico a CNN que se descubrió que este paciente tenía “un caso no diagnosticado de esclerosis múltiple”. Luego, el estudio realizó una “breve pausa del ensayo en julio mientras se realizaba una revisión de seguridad”, y un panel independiente concluyó que la afección “no estaba relacionada con la vacuna”, según el correo electrónico.
He aquí por qué una vacuna no detendrá la pandemia de Covid-19 de inmediato
Sin embargo, una versión anterior de una hoja de información para el participante enumera una afección neurológica diferente.Un voluntario en el ensayo “desarrolló síntomas de mielitis transversa (inflamación de la médula espinal)”, según la hoja de información del participante fechada el 12 de julio, que fue archivada en el registro ISRCTN, una base de datos de documentos relacionados con ensayos clínicos.Una hoja de información del participante fechada casi un mes después dice que un voluntario “desarrolló síntomas neurológicos” y que este voluntario “fue diagnosticado posteriormente con una enfermedad neurológica no relacionada”. En este documento, que está fechado el 5 de agosto, no queda claro si es el mismo voluntario que se describe en el documento de julio.Una hoja de información del participante más reciente , fechada el 11 de septiembre, no menciona ni la esclerosis múltiple ni la mielitis transversa, solo dice que los voluntarios tenían “síntomas neurológicos inexplicables que incluían cambios en la sensibilidad o debilidad de las extremidades”.Estos son los relatos que Krumholz, el médico de Yale, dijo que parecían inconsistentes. Dijo que aún no estaba claro si los participantes desarrollaron enfermedades similares que podrían haber sido causadas por la vacuna.”Todo esto es algo realmente importante”, dijo Krumholz, director del Centro de Investigación y Evaluación de Resultados en Yale.
El segundo participante enfermo
El 8 de septiembre, AstraZeneca dijo que la enfermedad de un voluntario en el Reino Unido había provocado una pausa en el juicio.Al principio, AstraZeneca y Oxford lo llamaron una “enfermedad inexplicable”.El ensayo se detuvo en todo el mundo mientras se investigaba la enfermedad. Cuatro días después, se anunció que el juicio se había reanudado en el Reino Unido.En ese momento, la universidad dijo que los datos de seguridad fueron revisados por un “comité de revisión de seguridad independiente y el regulador del Reino Unido, la MHRA”, la Agencia Reguladora de Medicamentos y Productos Sanitarios.El 17 de septiembre, CNN informó que un documento interno de AstraZeneca, etiquetado como “informe inicial”, decía que una voluntaria de 37 años previamente sana había sufrido mielitis transversa. El informe se envió a los médicos que administran los sitios de ensayos clínicos del estudio.
Transparencia vs confidencialidad
La hoja de participantes más reciente de Oxford dice que las enfermedades de los voluntarios se sometieron a una “revisión independiente” y se descubrió que “se consideró poco probable que estuvieran asociadas con la vacuna o que no había pruebas suficientes para decir con certeza que las enfermedades estaban o no relacionadas con la vacuna “.Pero no explican cómo llegaron los revisores a esa conclusión.

Se reanudará el ensayo de la vacuna Oxford de AstraZeneca, dice la universidad
El Dr. Paul Offit, experto en enfermedades infecciosas de la Universidad de Pensilvania, dijo que AstraZeneca y Oxford deberían explicar por qué consideran que las enfermedades no están relacionadas con la vacuna.”¿Qué tienen estos casos que los hace sentir cómodos de que estas enfermedades no fueron causadas por la vacuna?” él dijo. “Ellos conocen esta historia mejor que nosotros y deberían poder decir ‘nos sentimos cómodos de que estos casos no estuvieran relacionados con la vacuna debido a X”.Krumholz, el médico de Yale, estuvo de acuerdo. Se podría pedir a cientos de millones de personas que se tomen esta vacuna, y la información incompleta sobre las enfermedades de estos voluntarios solo generará dudas en la mente de las personas, dijo.”Realmente necesitan que la gente confíe en el proceso”, dijo.AstraZeneca y Oxford han declarado repetidamente que no pueden revelar cierta información debido a preocupaciones de confidencialidad para los participantes del estudio.Los científicos, sin embargo, dicen que la empresa y la universidad no han sido consistentes en la forma en que aplican estas preocupaciones de confidencialidad.Por ejemplo, AstraZeneca ni Oxford no han identificado el diagnóstico final del segundo voluntario, citando requisitos de confidencialidad.Pero AstraZeneca ha dado un diagnóstico, esclerosis múltiple, para el primer paciente. La empresa no ha explicado por qué las reglas de confidencialidad les impiden dar un diagnóstico para un paciente y no para el otro.La compañía no ha negado un informe en STAT News que dice que el CEO de AstraZeneca, Pascal Soriot, discutió el diagnóstico del segundo voluntario en una llamada telefónica con inversionistas.
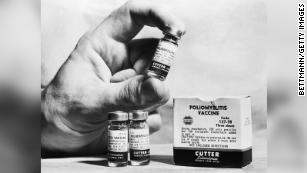
Los desastres de vacunas pasados muestran por qué apresurar una vacuna contra el coronavirus ahora sería ‘colosalmente estúpido
‘Los científicos dicen que están preocupados por las inconsistencias de la empresa.”Si no puede hablar debido a la confidencialidad, no lo haga frente a sus accionistas”, dijo Offit. “Esta elección de dar información incompleta o cambiante, ¿qué opinas de eso? No creo que puedas sacar nada de eso, aparte de que no estás recibiendo toda la historia”.Offit es miembro del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, que se espera que revise las solicitudes de las compañías farmacéuticas para comercializar vacunas contra el coronavirus.En un comunicado a CNN, AstraZeneca dijo que el 19 de septiembre publicaron el protocolo para su estudio. Otras dos empresas que desarrollan vacunas, Moderna y Pfizer, habían publicado sus protocolos dos días antes.”Dado el impacto global sin precedentes de la pandemia de coronavirus y la necesidad de información pública, AstraZeneca ha publicado el protocolo y diseño detallados de nuestro ensayo clínico AZD1222. Las buenas prácticas clínicas (BPC) y los estándares regulatorios dictan que la información que compartimos está estrictamente controlada para que para no influir indebidamente o sesgar los estudios clínicos. Normalmente, en el desarrollo clínico, los protocolos no se comparten, pero en este caso debido al mayor escrutinio que hemos compartido nuestro protocolo de la FDA de EE. UU.En un evento del jueves en el Foro Económico Mundial , Soriot, el CEO de AstraZeneca, dijo que su compañía ha estado considerando cuánta transparencia es posible brindar.
“Estamos considerando discutir con otras empresas como industria qué tipo de transparencia podríamos ofrecer sin comprometer la privacidad del paciente, por supuesto, pero también sin comprometer el ensayo en sí, porque si divulga la información, demasiada información, puede comprometer realmente el ensayo clínico en sí “.Agregó que una vez que los reguladores aprueban una vacuna, el público debe tener confianza en ella.”Realmente hay que amar las teorías de la conspiración para creer que todos los reguladores del mundo estarán de acuerdo en defender una vacuna que no es segura y eficaz”, dijo Soriot. “La gente tiene que aceptar que tiene que confiar en alguien en algún momento”.Offit dijo que si AstraZeneca va a revelar alguna información médica sobre los dos sujetos del estudio, debe quedar completamente claro sobre sus diagnósticos y lo que eso significa para la seguridad de la vacuna. “Esta elección de dar información incompleta o cambiante, ¿qué opinas de eso? No creo que puedas sacar nada de eso, aparte de que no estás entendiendo la historia completa”, dijo.
visita yodarta.org para más reportes que tu país esconde.
